Intramolekulare Wasserstoffbrücken in Aminosäuren.
 |
English version. |
| © |
Copyright-Hinweis. |
 |
Übersicht. |
Intramolekulare Wasserstoffbrücken in Aminosäuren. |
|
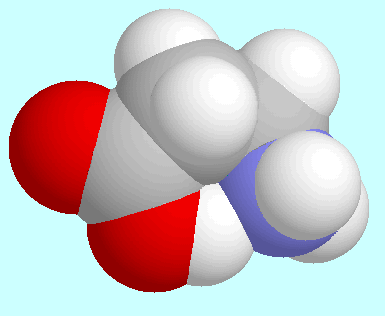
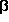 -Alanin bildet ein symmetrie-eindeutiges Konformer
mit einer O-H···N
Wasserstoffbrücke. Dieses Konformer hat eine unsymmetrische Geometrie
vom Umschlag-Typ: die Atome der COOH-Gruppe, das
-Alanin bildet ein symmetrie-eindeutiges Konformer
mit einer O-H···N
Wasserstoffbrücke. Dieses Konformer hat eine unsymmetrische Geometrie
vom Umschlag-Typ: die Atome der COOH-Gruppe, das  -Kohlenstoffatom
-Kohlenstoffatom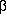 -Kohlenstoffatom
-Kohlenstoffatom
 Obwohl sie keine asymmetrischen Kohlenstoffatome
enthalten, bilden die beiden Konformere mit der
O-H···N Wasserstoffbrücke
ein Enantiomerenpaar, weil sie sich wie Bild und
Spiegelbild zueinander verhalten.
Das ist insoferne interessant, weil zwischen ihnen ein Reaktionsweg
besteht, der die Wasserstoffbrückenbindung intakt lässt. Der
Übergangszustand dieses Reaktionsweges ist nicht die
spiegelsymmetrische Anordnung, in der die Atomkette H-O-C-C-C-N ein
ebenes (aber unregelmäßes) Sechseck bildet. Statt dessen
gibt es zwei unsymmetrische Übergangszustände, in denen die
Aminogruppe um etwa 20° aus der spiegelsymmetrischen Anordnung
verdreht ist (im bzw. gegen den
Uhrzeigersinn). Daher gibt es auch zwei, hinsichtlich der
Energiebarriere äquivalente Reaktionswege, die beide
die Wasserstoffbrückenbindung aufrecht halten. Beide Wege vermeiden den
Punkt der Achiralität und bleiben so von Anfang bis Ende chiral,
wechseln aber zwischen Anfang und Ende die Händigkeit.
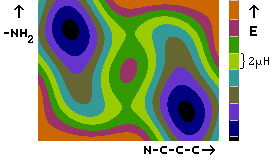
Der entsprechende Ausschnitt der Energiehyperfläche rund um diesen
achiralen Punkt ist neben diesem Absatz gezeigt.
Obwohl sie keine asymmetrischen Kohlenstoffatome
enthalten, bilden die beiden Konformere mit der
O-H···N Wasserstoffbrücke
ein Enantiomerenpaar, weil sie sich wie Bild und
Spiegelbild zueinander verhalten.
Das ist insoferne interessant, weil zwischen ihnen ein Reaktionsweg
besteht, der die Wasserstoffbrückenbindung intakt lässt. Der
Übergangszustand dieses Reaktionsweges ist nicht die
spiegelsymmetrische Anordnung, in der die Atomkette H-O-C-C-C-N ein
ebenes (aber unregelmäßes) Sechseck bildet. Statt dessen
gibt es zwei unsymmetrische Übergangszustände, in denen die
Aminogruppe um etwa 20° aus der spiegelsymmetrischen Anordnung
verdreht ist (im bzw. gegen den
Uhrzeigersinn). Daher gibt es auch zwei, hinsichtlich der
Energiebarriere äquivalente Reaktionswege, die beide
die Wasserstoffbrückenbindung aufrecht halten. Beide Wege vermeiden den
Punkt der Achiralität und bleiben so von Anfang bis Ende chiral,
wechseln aber zwischen Anfang und Ende die Händigkeit.
Der entsprechende Ausschnitt der Energiehyperfläche rund um diesen
achiralen Punkt ist neben diesem Absatz gezeigt.
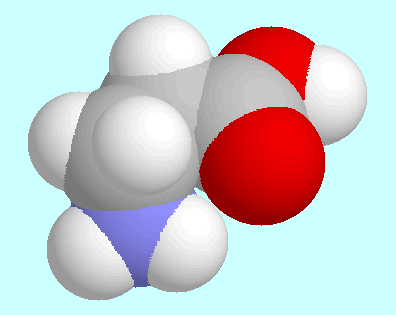 So wie in Glycin sind die Konformere mit der Wasserstoffbrücke
nicht die globalen Minima der Potenzialfläche. Der Grund dafür ist,
dass die COOH-Gruppe in der cis-Orientierung, in der die
Gruppen C=O und O-H auf der gleichen Seite der C-O-Bindung liegen,
etwa 35 kJ/mol stabiler ist als in der trans-Stellung.
Dadurch wird der Energiegewinn der Wasserstoffbrückenbindung von
etwa 32 kJ/mol mehr als zunichte gemacht.
Die Geometrie des globalen Minimums ist dadurch gekennzeichnet, dass
die COOH-Gruppe und die Kohlenstoffatome
So wie in Glycin sind die Konformere mit der Wasserstoffbrücke
nicht die globalen Minima der Potenzialfläche. Der Grund dafür ist,
dass die COOH-Gruppe in der cis-Orientierung, in der die
Gruppen C=O und O-H auf der gleichen Seite der C-O-Bindung liegen,
etwa 35 kJ/mol stabiler ist als in der trans-Stellung.
Dadurch wird der Energiegewinn der Wasserstoffbrückenbindung von
etwa 32 kJ/mol mehr als zunichte gemacht.
Die Geometrie des globalen Minimums ist dadurch gekennzeichnet, dass
die COOH-Gruppe und die Kohlenstoffatome
 und
und
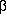 annähernd in einer Ebene liegen, aus der das Stickstoffatom herausragt.
Das Carbonylsauerstoffatom und ein Wasserstoff der Aminogruppe kommen
sich in dieser Anordnung nahe, aber nicht nahe genug um eine
Wasserstoffbrücke ausbilden zu können.
annähernd in einer Ebene liegen, aus der das Stickstoffatom herausragt.
Das Carbonylsauerstoffatom und ein Wasserstoff der Aminogruppe kommen
sich in dieser Anordnung nahe, aber nicht nahe genug um eine
Wasserstoffbrücke ausbilden zu können.
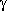 -Aminobuttersäure.
-Aminobuttersäure.