Intramolekulare Wasserstoffbrücken in Aminosäuren.
 |
English version. |
 |
Übersicht. |
Intramolekulare Wasserstoffbrücken in Aminosäuren. |
|
Aminosäuren
sind nicht nur die Bausteine für Peptide und Proteine, sondern
auch von großem Interesse für die Strukturchemie, weil sie im
festen Zustand und in polaren Lösungen Zwitterionen
H N
N -X-COO
-X-COO bilden, während in der
Gasphase oder in Matrixisolation neutrale Moleküle
bilden, während in der
Gasphase oder in Matrixisolation neutrale Moleküle
 N-X-COOH
N-X-COOH![]() Der Übergang vom Zwitterion zur Neutralform,
Animation für
Der Übergang vom Zwitterion zur Neutralform,
Animation für 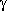 -Aminobuttersäure.)
-Aminobuttersäure.)
Da die meisten Aminosäuren sehr stabile Kristalle bilden, die sich noch vor dem Schmelzen zersetzen, sind experimentelle Studien an der Neutralform nur durch sehr aufwändige Verfahren möglich. Im Gegensatz dazu sind quantenchemische Molekülberechnungen das ideale Werkzeug zur Untersuchung derartiger Substanzen, weil diese Rechnungen gerade einzelne, isolierte Moleküle im Vakuum behandeln und Umgebungseinflüsse nur bedingt durch zusätzliche Terme berücksichtigt werden können.
Auf den folgenden Seiten sind
ausgewählte Ergebnisse von ab initio Untersuchungen
der Neutralform von  -Aminosäuren
-Aminosäuren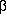 -Alanin,
-Alanin,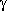 -Aminobuttersäure, ...)
-Aminobuttersäure, ...)